本文中,作者们对噬菌体的Qβ颗粒进行了结构分析和突变改造,提高了其诱导产生目的抗体的能力和专一性,并证明了其在疫苗设计中的普适性和应用潜力。
疫苗能够有效治疗和预防多种疾病,为了增加疫苗的安全性,人们将亚单位抗原与疫苗载体结合构建结合疫苗。结合疫苗中使用最多的抗原是肿瘤相关碳水化合物抗原(TACA),但TACA无法单独诱发有效的抗癌免疫反应,因而需要免疫载体的辅助,免疫载体可以起到递送抗原和增强疫苗免疫反应的作用。病毒样颗粒(VLP)是一类新型的用于疫苗设计的免疫原性载体,其中的噬菌体的Qβ颗粒也可用于疫苗载体,但Qβ还会诱导产生抗Qβ本身的抗体,可能会干扰机体对目标抗原的免疫响应。因此,作者们想根据Qβ的晶体结构进改造,从而提升其作为疫苗载体的性能和安全性。
首先,作者们测试了Qβ诱导抗TACA的IgG抗体的能力。他们选择了在人类癌症中广泛存在的Tn作为TACA的代表性抗原,先得到NHS-Tn衍生物,进而合成Qβ-Tn共轭物(wtQβ-Tn),质谱分析表明wtQβ-Tn的每个Qβ颗粒平均修饰有370个Tn。然后作者们分别在第0、14和28天向小鼠注射wtQβ-Tn或wtQβ,收集血液,利用BSA-Tn作为包被抗原进行抗Tn IgG抗体的ELISA分析。结果发现wtQβ-Tn可以诱发大量的抗Tn IgG抗体,证明Qβ确实是能够有效诱导抗Tn IgG抗体反应的优秀疫苗载体。此外作者也用Qβ作为包被抗原进行了ELISA分析,发现wtQβ-Tn还能够大量的抗Qβ抗体,并且随后实验表明抗Qβ抗体的产生无法通过异源Prime-Boost方案来减少,这不利于疫苗的开发。
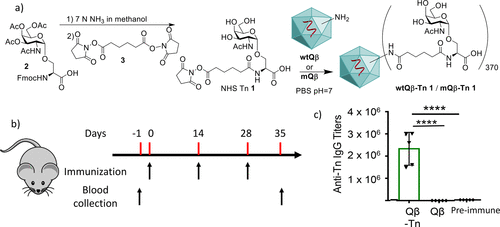
图1. Qβ是诱导抗Tn IgG抗体反应的强大载体
接下来作者尝试通过Qβ的结构分析和突变设计来降低其抗载体抗体的诱发水平。鉴于抗Qβ抗体的产生源于Qβ上的特异性B细胞识别表位,作者们制备了覆盖Qβ外壳蛋白的肽库并用ELISA进行筛选,结果表明:Qβ的B细胞表位并不是连续的线性氨基酸序列,有可能只是在蛋白的三维结构中彼此接近。为了指导Qβ的B细胞表位的分析和突变,作者借助XRD技术解出了Qβ外壳蛋白的晶体(PDB:7TJM),分辨率4.2 Å。接着他们计算了Qβ外壳蛋白每个残基的相对可及表面积(RASA),发现N10,K16,A38,T75和E103的RASA最大,是最靠近表面的残基。接着作者们利用DiscoTope 2.0(一个基于残基的表面可及性和空间邻域预测不连续B细胞表位的程序)对Qβ晶体结构进一步分析,得出结论:K16、A38、T75和E103最有可能位于Qβ的B细胞表位。作者们将A38、T75和E103突变为赖氨酸,从而破坏B细胞表位,同时这些突变后的赖氨酸还可以被Tn抗原偶联修饰,从而提高B细胞表位的屏蔽效果。除此之外,作者们发现引入A40C和D102C这两个突变可以使得Qβ二聚体的单体之间形成额外的二硫键,从而提高其热稳定性。
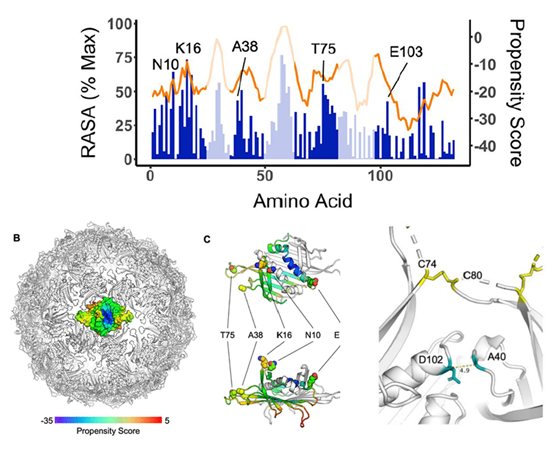
图2. Qβ结构分析和突变改造
基于前述发现,作者构建了一系列Qβ的突变体(A38K、T75K、A40C/D102C和A38K/A40C/D102C),称为mQβs。使用相同的方案和Tn偶联,并且保持各个突变体上Tn的修饰量与wtQβ-Tn基本相同,同样使用ELISA检测mQβ-Tn诱导抗体产生的能力。结果表明大多数突变均能产生更高水平的抗Tn IgG抗体,特别是mQβ(A38K/A40C/D102C)-Tn,它能诱导产生1.8×10 7个ELISA单位的抗Tn IgG抗体,比wtQβ-Tn高10倍,也是目前已经报道中最高的。除此之外,mQβ-Tn诱导产生的抗载体抗体的量也明显低于wtQβ-Tn。
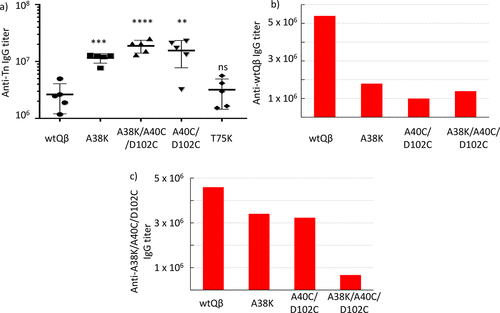
图3. Qβ作为Tn载体的性能评估
随后作者借助流式细胞术分析了mQβ(A38K/A40C/D102C)-Tn对表达Tn的肿瘤细胞的识别和结合能力。结果表明:由mQβ(A38K/A40C/D102C)-Tn引发的IgG抗体与TA3Ha细胞(表达有Tn抗原)的结合能力明显强于wtQβ-Tn。此外,作者还证明mQβ载体诱导抗Tn IgG抗体的能力也明显强于常见的基准蛋白载体(KLH、TT和CRM-197)。
接下来作者评估了mQβ作为疫苗载体的普适性。GD2是另一种常见的TACA抗原,它们借助类似策略合成了mQβ-GD2和wtQβ-GD2,证明mQβ同样能增强针对GD2抗原 的免疫反应。此外,他们还选择了SARS-CoV-2的RBD肽表位,证明mQβ偶联物还可以有效诱导产生靶向SARS-CoV-2相关肽抗原的抗体。上述分析表明mQβ可用作各类抗原疫苗的载体,具有很好的普适性。
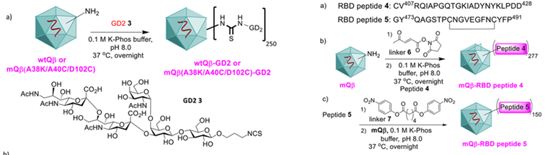
图4. Qβ还可用作GD2和新冠RBD肽段抗原的载体
最后作者评估了mQβ-Tn的体内疗效。他们在小鼠上接种TA3Ha肿瘤,然后使用mQβ-Tn,wtQβ-Tn联合环磷酰胺(CP)化疗进行治疗。结果表明:相比于单独的化疗,使用mQβ-Tn免疫治疗和CP化疗联用能够大大提高小鼠的存活率。

图5. mQβ-Tn可在小鼠中诱导抗癌免疫
总的来说,作者们析了Qβ的晶体结构并借助结构分析找到了上面可能的B细胞表位,通过在表位上引入突变等方法得到mQβ突变体。他们证明mQβ作为疫苗载体能更好地诱导抗目标抗原抗体的产生,并可减少不利的抗载体抗体的产生,具有一定的普适性,为下一代疫苗载体的开发提供了重要思路。
