文章标题是“A Capture Strategy for the Identification of Thio-Templated Metabolites”。
本文通讯作者是来自德克萨斯农工大学的Coran M. H. Watanabe教授,其课题组专注于天然产物生物合成及其作用机制方面的研究。
本文中,作者设计并合成了新型亲核化学探针,实现了天然产物合成过程中硫酯中间体的直接且有效的捕获。
以非核糖体肽(NRP)和多酮(PKs)结构为核心的天然产物,在抗生素、抗肿瘤药物和免疫抑制剂等诸多与疾病治疗密切相关的小分子的设计与开发中起着重要的作用。因此,为了更好地利用和挖掘这些天然产物,研究者试图对这一系列小分子的天然合成途径进行解析。然而,NRPs和PKs的合成多依赖于多结构域蛋白的循环催化作用,即其合成过程会伴随着底物-酶硫酯中间体的产生。然而,由于其反应活性高、稳定性低等问题,人们难以实现这类硫酯中间体的直接捕获。
研究者试图通过直接鉴定的策略,将预先鉴定到的用于产物合成的硫酯酶纯化后,在体外直接验证其反应机制,希望实现中间体的鉴定。然而,这一策略必须预先知道天然产物大致合成过程以及其对应的硫酯酶的种类,因此受到限制。基于传统质谱的鉴定策略受到检测极限和片段鉴定能力的影响,从而也无法满足有效检测的目的。基于酸/碱水解的策略可以将硫酯中间体转化成结构稳定的游离羧酸,以完成后续检测。但是并不是每一种系统都对这种水解模式敏感,且许多游离羧酸难以被LC-MS检测与电离,以至于无法广泛地应用。受到上述的诸多限制,研究者无法对具有重要疗效的天然产物的合成机制进行解析,因此,开发与建立一种普适性的硫酯中间体的直接捕获平台,具有极其重要的意义。
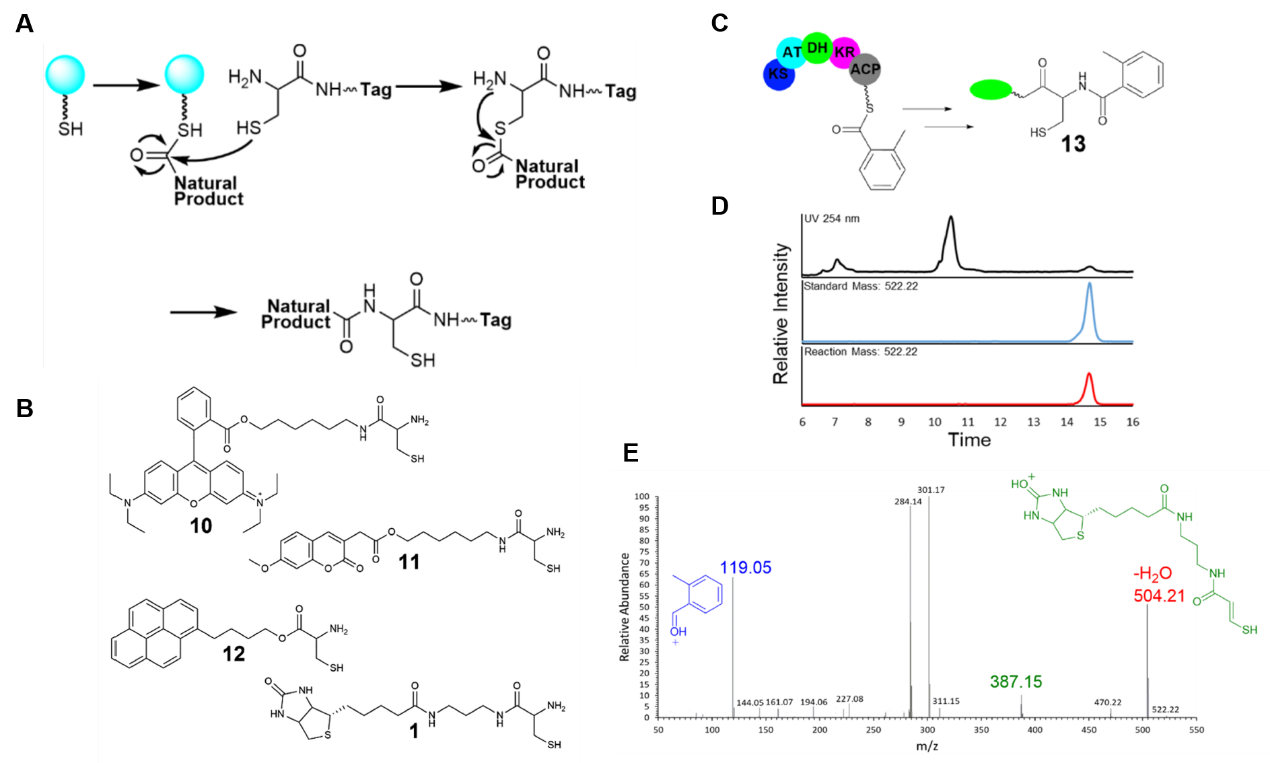
图1. A.硫酯中间体直接捕获策略示意图;B.纯化标签结构示意图;C. Biotin-Cys探针与AziB的理论反应式;D.通过LC-MS/MS对反应进行直接监测后,其对应的色谱结果显示,捕获的中间体与理论产物的出峰位置一致;E.通过LC-MS/MS对反应进行直接监测后,其对应的二级质谱结果显示,探针的结构组成与理论完全一致。
本文中,作者设计并开发了一种新型亲核性化学捕获探针(图1. A),希望实现硫酯中间体的捕获与鉴定。受到此前报道的硫酯化合物亲核裂解的策略的启发,他们设计了上述探针(图1. A)。探针主体包括半胱氨酸基团与纯化标签基团,其中半胱氨酸基团可以实现硫酯中间体的有效捕获,并增强其稳定性,而纯化标签基团为后续富集与鉴定提供了帮助。从机理上看,半胱氨酸中具有强亲核能力的巯基可以进攻硫酯键中的羰基部分,从而将中间体捕获。随后探针上邻近的氨基可以进行进一步进攻,引发重排反应并生成稳定的酰胺键。后续实验中,通过亲和纯化标签,研究者可以将产物从复杂体系中分离出来,实现中间体之间的鉴定。
为了验证这一探针的捕获能力,评价多种亲和纯化标签的表现效果(图1. B),作者将探针用于2-甲基苯甲酸产生系统中活性中间体的捕获实验中。结果显示,探针成功实现了中间体的捕获,且基于生物素基团的标签具有最好的表现效果。因此,他们合成了基于生物素的亲核探针Biotin-Cys用于之后的实验中,并通过LC-MS/MS对AziB与其底物形成的活性中间体进行分析(图1. C)。色谱结果显示,中间体被有效捕获(图1. D),而二级质谱结果显示,产物的结构信息与理论完全一致(图1. E)。由此,这一探针的硫酯中间体鉴定能力得到了证明。
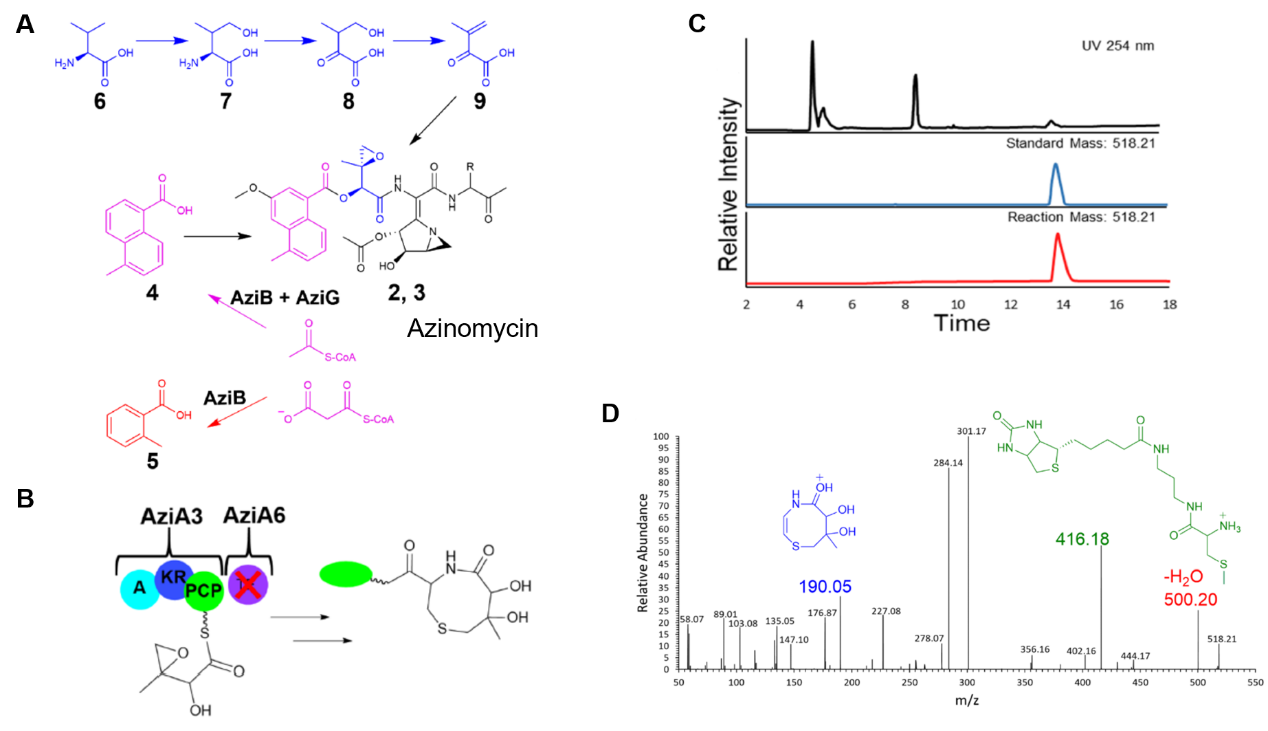
图2. A. Azinomycin天然生物合成路线图;B. Biotin-Cys探针与AziA3相关中间体的理论反应式;C.通过LC-MS/MS对反应进行直接监测后,其对应的色谱结果显示,捕获的中间体与理论产物的出峰位置一致;D.通过LC-MS/MS对反应进行直接监测后,其对应的二级质谱结果显示,探针的结构组成与理论完全一致。
基于这一结果,他们进一步将Biotin-Cys探针用于天然产物Azinomycin产生过程中的硫酯中间体的鉴定与表征实验中(图2. A)。之前的研究中指出,Azinomycin由于其具有的抗肿瘤活性,而受到广泛的关注。然而,其天然合成过程中的羰基还原反应和环氧基团形成过程的顺序还未被解析,而解析的关键在于能否对其对应的硫酯中间产物进行结构解析(图2. A)。这一关键产物对应的酶是具有羰基还原能力的AziA3,且之前的报道中指出,还原反应发生的同时,AziA3与底物以硫酯键共价连接。于是他们将纯化好的,结合了关键硫酯中间体的AziA3进行了纯化,并加入探针进行体外的捕获(图2. B)。LC-MS/MS和NMR的结果显示,他们成功捕获了中间体,并且探针的巯基与中间体还可以进一步反应,使得环氧结构打开,得到了其对应八元环特征产物(图2. C-D)。对结果进行分析,中间体形成时,羰基被还原时,环氧结构就已经存在了,且还能够与探针的巯基进行反应。由此可知,环氧化结构的形成先于羰基还原反应的发生。至此,探针的中间体捕获能力以及深度解析反应机制的能力都得到了再次证明。
探针的检测深度得到了证明,而作者还试图展示其检测的普适性。他们将探针应用于大肠杆菌素colibactin合成过程中的基于NRPS ClbN的中间体的鉴定与表征过程中(图3. A-B)。结果显示,在体外纯化的体系中,探针成功捕获辛酰天冬氨酸中间体,并且以16和17两种形式而被检测和表征。
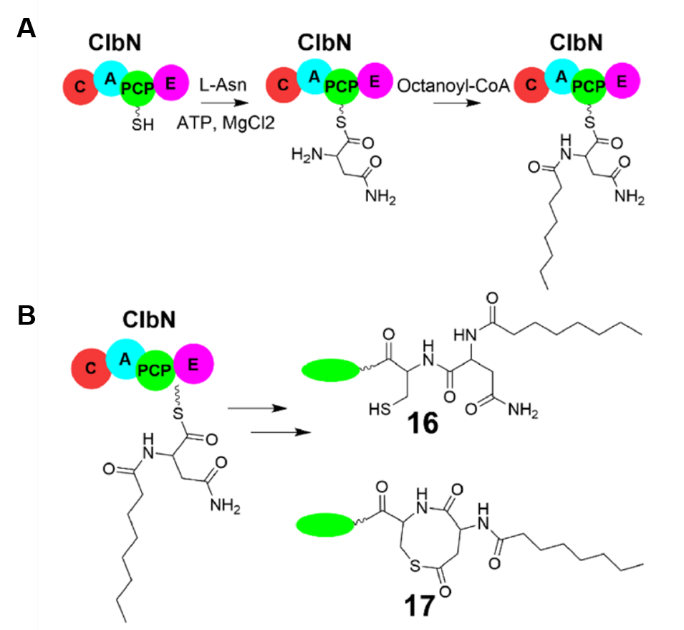
图3. A. Colibactin天然生物合成过程中,基于硫酯中间体的反应示意图;B. Biotin-Cys探针对ClbN相关硫酯中间体捕获的理论反应式。
综上,作者设计并开发了一种亲核性化学探针的硫酯中间产物普适性捕获策略,并且能够从反应体系中实现目标中间体的捕获与表征,具有在原生体系中解析天然产物形成机制与结构、功能的潜力。在上述的工作中,他们实现了Azinomycin和colibactin天然合成过程中的硫酯中间体的鉴定与表征,为反应机理的解析提供了理论与实验基础。在理想情况下,这一策略将有助于在生物体系中筛选和鉴定新的生物活性天然产物,对治疗药物的开发具有重要意义。
