当你因饥饿辗转反侧、彻夜难眠时,你是否也曾拜倒在零食的石榴裙下,又或是打开手机迅速下单一份香喷喷的夜宵呢?其实这是你下丘脑中的AGRP神经元(表达刺鼠相关肽)在作祟。这些对饥饿敏感的AGRP神经元负责让你产生难以忍耐的饥饿感,从而激励你对食物伸出罪恶的小手。神奇的是,这些饥饿时非常活跃的AGRP神经元在找到食物后,就会进入低活性的休眠状态[1]。
这些AGRP神经元上还表达了LEPR(即大名鼎鼎的瘦素受体),当AGRP神经元活性过高时,会引发小鼠食欲过剩和高血糖的现象[2]。这也与人类患者中瘦素及其受体功能紊乱后易引发肥胖、糖尿病等病症的情况十分相似。
怎样才能让“激动不已”的AGRP神经元重返平静呢?科学家们发现了三套解决方案:首先是依赖于感觉信号的对食物的探测;其次是肠道对营养物质的响应;最后是能量平衡的恢复。而这三套方案所需的时间依次递减,显然快速找到食物是迅速让AGRP神经元偃旗息鼓的最佳方案。然而这个现象背后的分子机制仍是迷雾重重。
近日发表于Nature的一篇文章证明,LHVGLUT2→DMHLEPR→AGRP神经环路可以被环境信号引导的食物获取所激活,从而迅速降低AGRP神经元活性。
研究人员认为,AGRP神经元对食物线索的快速响应很可能是由其上游的传入信号所支配的。在AGRP神经元上游的神经通路中,有一类位于腹侧下丘脑的表达瘦素受体(LEPR)和强啡肽原的GABA能神经元,即DMHLEPR神经元被发现由食物的感官探测激活。
为了证实食物探测的感觉信号和神经元之间的相关性,研究者们对饥肠辘辘的小鼠进行了训练,灯光亮起就意味着“放饭”,经过训练的小鼠可以迅速选择亮灯的一侧。相比对照组小鼠,这些经过训练的小鼠在光刺激后,DMHLEPR神经元活性显著上升(图1)。
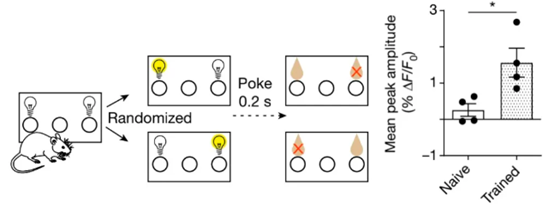
图1习得性食物线索对DMHLEPR神经元的调控作用
为什么发现食物的蛛丝马迹会让DMHLEPR神经元如此激动呢?研究人员利用逆向病毒追踪技术,发现了为DMHLEPR神经元动员的上游神经元——LHVGLUT2神经元。
随后,研究者们将依赖于Cre表达ChR2的AAV病毒(AAV-DIO-ChR2病毒)注射入Vglut2-IRES-Cre小鼠的双侧LHVGLUT2神经元,利用光遗传学手段,特异性激活LHVGLUT2→DMH的轴突终末,小鼠果然变得食欲不振(图2)。
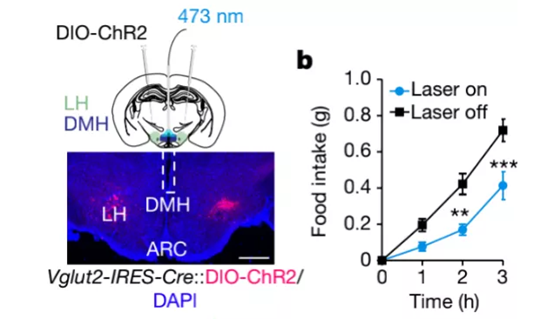
图2光遗传学激活LHVGLUT2→DMH轴突终末降低小鼠食物摄入量
那么,LH的传入信号是否真的会对下游DMHLEPR神经元和AGRP神经元产生直接影响呢?研究者们向Lepr-IRES-Cre小鼠的DMH区注射逆向的AAV-FlpO和AAV-DIO-GCaMP6,并向LH区注射AAV-fDIO-hM4Di,当用CNO处理后,可实现特异性抑制LH→DMH的传入。
此时,被食物线索激活的DMHLEPR神经元反应大大减轻(图3)。当选择性抑制LHVGLUT2神经元时,AGRP神经元被食物线索诱发的快速反应也同样被削弱。
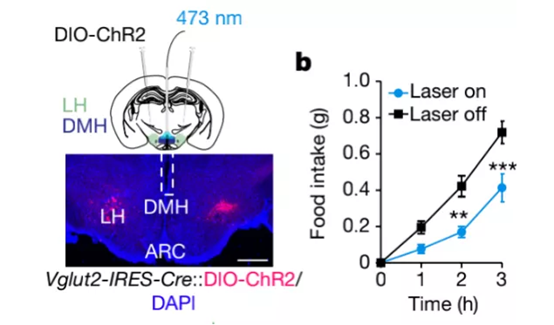
图3化学遗传抑制LH的传入降低DMHLEPR神经元对食物线索的反应性
这条由食物线索介导的调控通路(LHVGLUT2→DMHLEPR→AGRP)在小鼠的摄食行为中又扮演着怎样的角色呢?
研究者们将AAV-DIO-TeNT病毒注射入Lepr-IRES-Cre小鼠的DMHLEPR神经元,消除DMHLEPR突触释放,并对这些小鼠进行了图1所示的训练。
相比对照组,这些小鼠似乎变笨了,它们学会“灯光=食物”指令明显慢于对照组小鼠(图4)。同时,它们在学习过程中犯的错误也更多,反应的时间也更长了。
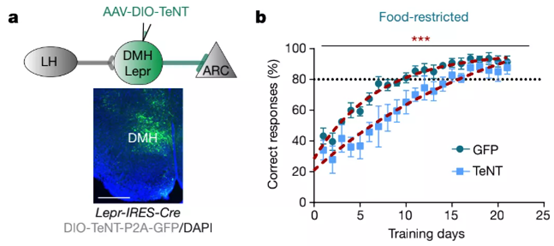
图4抑制DMHLEPR神经元信号传递的小鼠需要更长的学习时间
近日,另一篇发表于Current Biology的研究也同样聚焦于AGRP神经元和LH神经元之间的联系[2],研究者通过训练小鼠学会饥饿和饱食状态的行为范式,发现了似乎下丘脑对于“吃饱”(即为了维持能量平衡而进行的稳态进食)和“吃好”(即为了产生奖赏或降低厌恶的享乐进食)的调控存在分歧,也反应了摄食行为调控的复杂性。
总之,饥饿感使下丘脑AGRP神经元激活,产生了厌恶感,而食物线索可以激活LHVGLUT2→DMHLEPR→AGRP神经环路,减轻这种厌恶感。有趣的是,当这条通路被激活时,小鼠对于食物线索的学习能力显著上升。看来有时饿肚子也确实是“变聪明”的捷径呀。
参考文献
[1] Betley, J. N. , et al. "Neurons for hunger and thirst transmit a negative-valence teaching signal." Nature 521.7551(2015):180.
[2] Xu, J., Bartolome, C.L., Low, C.S. et al. Genetic identification of leptin neural circuits in energy and glucose homeostases. Nature 556, 505–509 (2018).
[3] Hypothalamic control of interoceptive hunger. Current Biology 2d Half(2021).
来源:转载于brainnews
